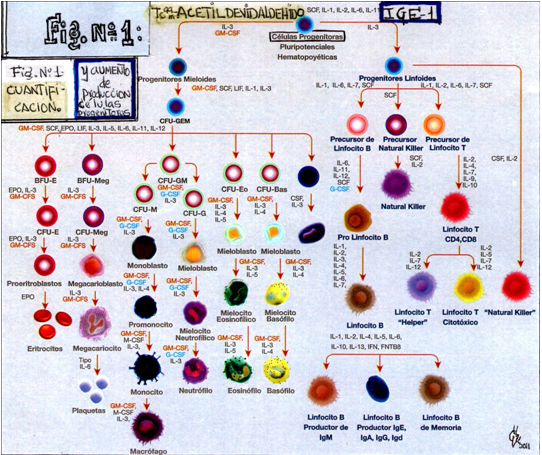
Valentín Cardona Ramírez
23 / abril / 2001
Introducción:
 Se representa un método para la detección de virus rábico, a la brevedad posible si el animal agresor está infectado de virus rábico.
Se representa un método para la detección de virus rábico, a la brevedad posible si el animal agresor está infectado de virus rábico.
La detección del virus rábico se lleva a cabo con facilidad. Consiste en preparar improntas de cerebro infectado y tratarlas con una suspensión de anticuerpos antirrábicos marcados con I-131. Posteriormente se detecta el anticuerpo unido al virus con un detector de radiaciones gamma como el que se usa para la captación de yodo de la glándula tiroides.
Material y Equipo:
1. Portaobjetos
2. Equipo de disección
3. Baño María
4. Pipetas Pasteur.
5. Abatelenguas
6. Cubeta de Coplin
7. Congelador (-20° C)
8. Contador gamma
Reactivos:
(Phosphate Buffer Solution PH 7.2)
Método:
 Se preparan dos lotes de ratones Albino Suizo de 23 días de edad; cada uno de los ratones de uno de los lotes se inocula con 0.03 ml. de una suspensión de CVS al 20 %; los ratones del lote restante no inoculados son testigo. Se proporciona a todos los animales agua y alimento ad libitum y cuando los ratones inoculados presentan la sintomatología característica de la rabia, se sacrifican.
Se preparan dos lotes de ratones Albino Suizo de 23 días de edad; cada uno de los ratones de uno de los lotes se inocula con 0.03 ml. de una suspensión de CVS al 20 %; los ratones del lote restante no inoculados son testigo. Se proporciona a todos los animales agua y alimento ad libitum y cuando los ratones inoculados presentan la sintomatología característica de la rabia, se sacrifican.
Toma de muestras:
Se extrae el cerebro del animal rabioso o sospechosos con tijeras estériles. Se hace un corte longitudinal en cara dorsal de cada hemisferio cerebral aproximadamente 2 mm de la cisura longitudinal o línea media del cerebro.El corte para el polo occipital del hemisferio y se extiende de 2 a 3 mm hacia delante; en profundidad atraviesa la sustancia blanca, hasta alcanzar un espacio estrecho, que es el hemisferio y aparece el Cuerno de Ammon, como un cuerpo semicilíndrico, blanco y brillante que sobresale lateralmente en el suelo del ventrículo. Tiene un contorno espiral y en el corte transversal presenta una superficie ondulada típica; el Cuerno de Ammon suele ser la mejor zona del cerebro para observar el virus rábico en los animales rabiosos de la mayoría de las especies.
Impresión, fijación del tejido y detección:
1. De cada uno de los cerebros, tanto sanos (testigos) como infectados de virus rábico se hacen improntas en juegos dobles de laminillas de vidrio; en primer lugar del Cuerno de Ammon, después de la corteza cerebral y finalmente del cerebelo.
2. Se obtiene pequeños cortes trasversales de 2 a 3 mm de grosor, se colocan sobre un depresor de lengua de madera, con la superficie del corte hacia arriba.
3. Se aplica un portaobjeto limpio sobre la superficie del corte de la pieza y presionando con suavidad hacia abajo, sólo lo necesario para que quede sobre el vidrio una impresión ligera de la superficie expuesta del tejido.
4. Las improntas se secan al aire, se colocan en una cubeta de Coplin, se cubren acetona fría y se mantienen 4 horas en un congelador (-15° C a -20° C).
 5. Una vez fijada las improntas con acetona, se dejan secar al aire libre, se delimitan en el portaobjetos con un marcador o con barniz de uñas y se conservan a -20° C por varios meses y se usan cuando sea necesario.
5. Una vez fijada las improntas con acetona, se dejan secar al aire libre, se delimitan en el portaobjetos con un marcador o con barniz de uñas y se conservan a -20° C por varios meses y se usan cuando sea necesario.
6. Si se desea hacer una detección, se vierten 6 gotas de AC-AR-I-131 de anticuerpos antirrábicos marcados con I-131 que deben disponerse en cada centro de detección, a cada una de las improntas y se colocan en cajas de Petri húmedas, mojando el papel que tiene la tapa y se introducen a un baño María a 37° C durante 30 minutos.
7. Después de la incubación se levan las preparaciones con agua destilada para eliminar el exceso de anticuerpos no unidos al virus presente en la impronta.
8. Se colocan en la cubeta de Coplin que contiene PBS solución amortiguadora y se incuba a temperatura ambiente una hora; cada 15 minutos se agitan con suavidad.
9. Después de extraen y se enjuagan con agua destilada.
10. Se dejan reposar en la cubeta de Coplin que contiene agua destilada, 15 minutos a temperatura ambiente.
11. Se dejan secar al aire.
12. Se pasan una a una las laminillas a través de un detector de radiación gamma.
Deben elaborarse dos tablas:
Tabla I. Resultados.
Lectura de radiación emitida en cuentas por minuto (cpm) de las preparaciones de cerebro de animal rabioso.
|
Lecturas en c.p.m. |
|||||||
|
Muestras |
1 |
2 |
3 |
4 |
Suma |
Media |
|
|
Virus rábico |
VR-1 |
2975 |
3015 |
2965 |
3033 |
11988 |
2997 |
|
Virus rábico |
VR-1′ |
1567 |
1663 |
1723 |
1669 |
6622 |
1655 |
|
Virus rábico |
VR-2 |
3753 |
3775 |
3683 |
3651 |
14862 |
3715 |
|
Virus rábico |
VR-2′ |
18775 |
18419 |
18671 |
18449 |
74314 |
18578 |
|
Virus rábico |
VR-3 |
773 |
703 |
741 |
703 |
2920 |
730 |
|
Virus rábico |
VR-3′ |
1419 |
1305 |
1403 |
1415 |
5542 |
1385 |
|
Virus rábico |
VR-4 |
423 |
431 |
401 |
483 |
1738 |
434 |
|
Virus rábico |
VR-4′ |
527 |
575 |
497 |
461 |
2060 |
515 |
|
Virus rábico |
S-1 |
409 |
425 |
475 |
429 |
1738 |
434 |
|
Suma |
31102 |
30274 |
30998 |
30784 |
123608 |
||
|
Gran media |
3,090
|
||||||
Tabla II.
Lecturas de radiación emitidas en cuentas por minuto de las preparaciones de cerebro de animal sano con anticuerpos antirrábicos marcados con I-131.
|
Muestras |
Lecturas (cpm) |
|||||||
|
Virus rábico |
VR-1 |
152 |
148 |
126 |
98 |
131 |
655 |
131 |
|
Virus rábico |
VR-1′ |
262 |
302 |
338 |
286 |
(297) |
1485 |
297 |
|
Virus rábico |
VR-2 |
204 |
208 |
150 |
184 |
216 |
962 |
192 |
|
Virus rábico |
VR-3 |
248 |
244 |
174 |
228 |
250 |
1144 |
229 |
|
Virus rábico |
VR-3′ |
264 |
242 |
244 |
262 |
(253) |
1265 |
253 |
|
Virus rábico |
VR-4 |
348 |
332 |
338 |
298 |
(329) |
1645 |
329 |
|
Virus rábico |
VR-4′ |
312 |
304 |
356 |
314 |
(322) |
1608 |
322 |
|
Virus rábico |
VR-5 |
214 |
216 |
174 |
244 |
(212) |
1060 |
212 |
|
Virus rábico |
VR-5′ |
386 |
314 |
326 |
328 |
378 |
1732 |
346 |
|
Virus rábico |
VR-6 |
876 |
822 |
876 |
798 |
(843) |
4215 |
843 |
|
Virus rábico |
VR-6′ |
822 |
776 |
712 |
800 |
852 |
3962 |
792 |
|
Virus rábico |
S-1 |
232 |
264 |
216 |
202 |
(228) |
1142 |
228 |
|
Virus rábico |
S-2 |
300 |
274 |
240 |
270 |
(271) |
1355 |
271 |
Comentarios:
De los resultados en las tablas I y II observan diferencias significativas ya que las laminillas de tejido cerebral sano (S) muestran menor número de cpm emitidas, y el tejido cerebral que contiene virus rábico tiene mayor capacidad para fijar anticuerpos antirrábicos marcados con I-131, de esta manera presentan en la Tabla I una menor cantidad de radiación emitida en cuentas por minuto.Debe esperarse que las laminillas preparadas con cerebro de animal infectado con virus rábico, muestran una emisión en cuentas por minuto con diferencia significativa respecto a las laminillas preparadas con cerebro de animal sano. Y las laminillas preparadas con cerebro de animal sano no mostrarán diferencias significativas entre si .
Conclusión:
El método aquí descrito es simple, y su evaluación es objetiva para el diagnóstico porque no depende de la observación del ojo humano.De lo que procede se concluye que el método expuesto es una fuente de apoyo para detectar virus en cerebros de humanos y animales rabiosos.
APENDICE A. Marcado de anticuerpos antirrábicos con I-131.
Materiales y equipo:
1. Suero antirrábico de equipo ( frasco ámpula con 1000 UT)
2. Centrífuga.
3. Refrigerador (4° C).
4. Campana para iodinación.
5. Contador de radiaciones gamma tipo captador I-131.
6. Micropipeta
7. Tubos Eppendorrf de 1.5 ml con tapa
8. Tubo de ensayo de vidrio de 12 x 75 mm
9. Pipetas Pasteur
10. Punzón metálico
11. Lana de vidrio
Reactivos y preparación de la columna cromatográfica:
 Reactivos:
Reactivos:
1. Yodo-131 (NaI*)
2. Yodo-cuentas (Yodo Beads)
3. PBS (Phosphatte Buffer Solution) a PH 7.2:
NaCl ……………………………………. 0.8 g
KCl …………………………………….. 0.02 g
Na2HPO47H2O ………..……………. 0.215 g
Na2H2PO4 ……………………………. 0.02 g
H2O destilada …………………..……. 100 ml
4. Sephadex G-25-50
Preparación de la columna cromatográfica:
-
Se pesan 2 gr de Sephadex G-25-50 y se hidratan agregando agua destilada y se deja reposar en el refrigerador por 3 días, durante los cuales, diariamente, se decanta el sobrante, se adiciona un volumen de agua destilada igual al volumen decantado.
-
Se perfora el fondo de un tubo Eppendorf con un punzón metálico para obtener un diámetro aproximado de 2 mm y se usa lana de vidrio como soporte en el fondo del tubo.
-
Se agrega PBS hasta cubrir la tercera parte del tubo e inmediatamente después se agrega Sephadex G-25–50 previamente hidratado empacado uniformemente hasta aproximadamente tres cuartas partes de su capacidad, y se añade PBS hasta el borde del tubo.
-
Se almacena dentro del tubo de ensayo, que contenga PBS a un nivel superior al de la columna en refrigeración.
-
Al momento de usar; se extrae la columna del tubo de ensayo, se coloca en otro tubo de ensayo y se centrifuga a 1000 RPM durante un minuto, a fin de eliminar el volumen de exclusión.
Procedimiento de marcado de anticuerpos antirrábicos con *I-131. Se emplea la técnica de marcado en fase sólida usando Iodo-Cuentas (Markwell, 1982).
1. Se mide la radiactividad inicial del I-131 (0.2 ml./1.2 mCi) que está contenido en un tubo Eppendorf con tapa de 1.5 ml, en un contador gamma, en cm cpm.
2. Se agrega al tubo anterior el anticuerpo 0.45 ml./80 UI. (Se disuelve el anticuerpo liofilizado del frasco ámpula con 5 ml de PBS, obteniéndose así una solución que contiene 200 UI/ml)
3. Se agregan dos Iodos-cuentas.
4. Se agita suavemente y se deja reaccionar durante 15 minutos a temperatura ambiente, bajo una campana de iodinación.
5. Una vez transcurrido ese tiempo, se pasa la mezcla a la columna de Sephadex, a fin de separar el yodo libre de los anticuerpos antirrábicos.
6. Se centrifuga a 2000 RPM durante 2 minutos, la columna de Sephadex sobre un vial cilíndrico de fondo plano para así recuperar la proteína marcada en el fondo del tubo, el cual se lleva al contador gamma en donde se registra la actividad en cpm. Estos anticuerpos marcados se conservan en el refrigerador.
Cálculos para determinar la eficacia del marcador.
1. En un tubo Eppendorf se pone:
5.0 ml de PBS frío.
0.2 ml. de suero de paciente (normal)
2.0 m l de proteína iodinada (marcada)
2. Del tubo anterior (1) (PBS-suero- proteína I-131) se toman alicuotas preparadas por duplicado:
2 tubos con: 5 ml de tubo (1)
0.5 de ácido tricloroacético al 20% (TCA 20%)
2 tubos con: 0.5 ml del tubo (1)
0.5 ml. de PBS.
a) % del Yodo-131 unido a proteína = ![]()
b) La cantidad de radioiodo en la alicuota de proteína iodinada es: cpm – PBS – cpm TCA.
c) Eficacia de la reacción de iodinación es:
![]()
Los incisos a), b) y c) surgen de la siguientes preguntas:
I. ¿Cuánto radioiodo se tiene en: a) proteína iodinada, b)
¿Cuál es la eficacia de la reacción de iodinación? Esto es, ¿Qué cantidad de radioiodo original se une a la práctica?.
II. ¿Qué cantidad de proteína se recupera?
III. ¿Cuál es la actividad especifica de la proteína iodinada? (Con los valores 1 y 2 se estima)
Bibliografía:
1. Biofísica y Bioquímica del Virus Rábico en Interacción con la Célula Huésped Valentín Cardona Ramírez. Edit y Pub. SA de CV, Ahuehuetes No. 42, La Guadalupana, Xochimilco, DF. C.P. 16070, México 1994.
2. Antonio Morilla G y Carlos R Bautista Manual de Inmunología Edit. Diana 1986.
3. Markwell M.A.K. A New Solid State Reagente to Iodinante Proteíns, Anl. Bioch, 1982,125: 427.
4. Radioiodinación. Inmuno Chemistry in Practicle, John Staon /Thorpe, Blackwell Sci. Pub. 1987.
5. RIA Análisis de Radioreceptores en el Laboratorio de Inmunología Clínica. Edit. Médica Panamericana 1984.